Аўтар:
Mark Sanchez
Дата Стварэння:
3 Студзень 2021
Дата Абнаўлення:
1 Ліпень 2024

Задаволены
- крокі
- Метад 1 з 2: Вызначэнне масавага адсотка па зададзеных масам
- Метад 2 з 2: Вызначэнне масавага адсотка, калі масы не зададзены
Масавы працэнт задае адсоткавыя суадносіны элементаў у хімічным злучэнні. Для знаходжання масавага адсотка неабходна ведаць малярная маса (у грамах на моль) ўваходзяць у злучэнне элементаў або колькасць грамаў кожнага кампанента, неабходнае для таго, каб атрымаць зададзены раствор.Масавы працэнт вылічаецца даволі проста: дастаткова падзяліць масу элемента (або кампанента) на масу ўсяго злучэння (або раствора).
крокі
Метад 1 з 2: Вызначэнне масавага адсотка па зададзеных масам
 1 Выберыце раўнанне для вызначэння масавага адсотка хімічнага злучэння. Масавы працэнт знаходзіцца па наступнай формуле: масавы адсотак = (маса кампанента / агульная маса злучэння) x 100. Для атрымання адсоткаў вынік дзялення памнажаецца на 100.
1 Выберыце раўнанне для вызначэння масавага адсотка хімічнага злучэння. Масавы працэнт знаходзіцца па наступнай формуле: масавы адсотак = (маса кампанента / агульная маса злучэння) x 100. Для атрымання адсоткаў вынік дзялення памнажаецца на 100. - У пачатку рашэння задачы запішыце роўнасць: масавы працэнт = (маса кампанента / агульная маса злучэння) x 100.
- Маса які цікавіць вас кампанента павінна быць ва ўмове задачы. Калі маса не дадзена, перайдзіце да наступнага падзелу, у якім расказана пра тое, як вызначаць масавы адсотак пры невядомай масе.
- Агульная маса хімічнага злучэння знаходзіцца шляхам складання мас ўсіх элементаў (кампанентаў), якія ўваходзяць у склад гэтага злучэння (або раствора).
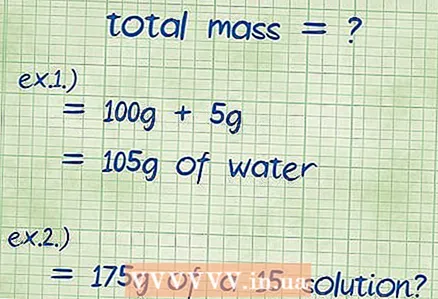 2 Вылічыце агульную масу злучэння. Калі вы ведаеце масы ўсіх складнікаў злучэнне кампанентаў, проста складзеце іх, і такім чынам вы знойдзеце агульную масу атрыманага злучэння або раствора. Гэтую масу вы выкарыстоўваеце ў якасці назоўніка ў раўнанні для масавага працэнта.
2 Вылічыце агульную масу злучэння. Калі вы ведаеце масы ўсіх складнікаў злучэнне кампанентаў, проста складзеце іх, і такім чынам вы знойдзеце агульную масу атрыманага злучэння або раствора. Гэтую масу вы выкарыстоўваеце ў якасці назоўніка ў раўнанні для масавага працэнта. - Прыклад 1: Чаму роўны масавы працэнт 5 грамаў гідраксіду натрыю, растворанага ў 100 грамах вады?
- Агульная маса раствора роўная суме колькасці гідраксіду натрыю і вады: 100 г + 5 г даюць 105 г.
- Прыклад 2: Колькі хларыду натрыю і вады неабходна для атрымання 175 грамаў 15-працэнтнага раствора?
- У гэтым прыкладзе дадзены агульная маса і неабходны працэнт, і патрабуецца знайсці колькасць рэчыва, якое неабходна дадаць у раствор. Пры гэтым агульная маса складае 175 грамаў.
- Прыклад 1: Чаму роўны масавы працэнт 5 грамаў гідраксіду натрыю, растворанага ў 100 грамах вады?
 3 Вызначце масу зададзенага кампанента. Калі вас просяць вылічыць "масавы працэнт", варта знайсці, колькі адсоткаў ад агульнай масы рэчыва складае маса пэўнага кампанента. Запішыце масу зададзенага кампанента. Гэта будзе лічнік ў формуле для масавага працэнта.
3 Вызначце масу зададзенага кампанента. Калі вас просяць вылічыць "масавы працэнт", варта знайсці, колькі адсоткаў ад агульнай масы рэчыва складае маса пэўнага кампанента. Запішыце масу зададзенага кампанента. Гэта будзе лічнік ў формуле для масавага працэнта. - Прыклад 1: маса зададзенага кампанента - гідрахларыд натрыю - складае 5 грамаў.
- Прыклад 2: у гэтым прыкладзе маса зададзенага кампанента невядомая, і яе варта знайсці.
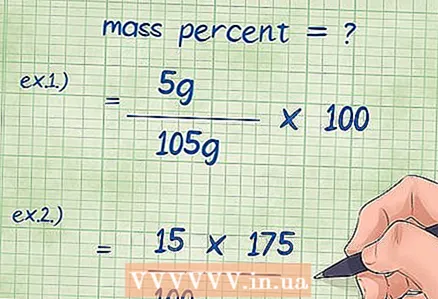 4 Падстаўце значэння ў раўнанне для масавага працэнта. Пасля таго як вы вызначыце ўсе неабходныя велічыні, падстаўце іх у формулу.
4 Падстаўце значэння ў раўнанне для масавага працэнта. Пасля таго як вы вызначыце ўсе неабходныя велічыні, падстаўце іх у формулу. - Прыклад 1: масавы адсотак = (маса кампанента / агульная маса злучэння) x 100 = (5 г / 105 г) x 100.
- Прыклад 2: неабходна пераўтварыць формулу для масавага адсотка так, каб можна было знайсці невядомую масу хімічнага кампанента: маса кампанента = (масавы адсотак * агульная маса злучэння) / 100 = (15 * 175) / 100.
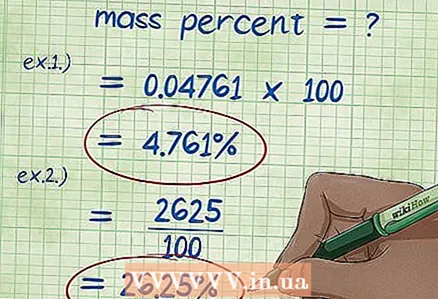 5 Вылічыце масавы працэнт. Пасля падстаноўкі ўсіх значэнняў у формулу для масавага адсотка зрабіце неабходныя вылічэнні. Падзяліце масу кампанента на агульную масу хімічнага злучэння або раствора і памножце на 100. У выніку ў вас атрымаецца масавы працэнт дадзенага кампанента.
5 Вылічыце масавы працэнт. Пасля падстаноўкі ўсіх значэнняў у формулу для масавага адсотка зрабіце неабходныя вылічэнні. Падзяліце масу кампанента на агульную масу хімічнага злучэння або раствора і памножце на 100. У выніку ў вас атрымаецца масавы працэнт дадзенага кампанента. - Прыклад 1: (5/105) x 100 = 0,04761 x 100 = 4,761%. Такім чынам, масавы працэнт 5 грамаў гідрахларыд натрыю, растворанага ў 100 грамах вады, складае 4,761%.
- Прыклад 2: перапісанае выраз для масавага адсотка кампаненты мае выгляд (масавы адсотак * агульная маса рэчыва) / 100, адкуль знаходзім: (15 * 175) / 100 = (2625) / 100 = 26,25 грамаў хларыду натрыю.
- Неабходную колькасць вады знаходзім шляхам адымання масы кампанента з агульнай масы раствора: 175 - 26,25 = 148,75 грамаў вады.
Метад 2 з 2: Вызначэнне масавага адсотка, калі масы не зададзены
 1 Выберыце формулу для масавага адсотка хімічнага злучэння. Асноўнае раўнанне для знаходжання масавага адсотка выглядае наступным чынам: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100. Малярная маса рэчыва - гэта маса аднаго молячы дадзенага рэчыва, у той час як малекулярная маса ўяўляе сабой масу аднаго молячы усяго хімічнага злучэння. Каб атрымаць працэнты, вынік дзялення памнажаецца на 100.
1 Выберыце формулу для масавага адсотка хімічнага злучэння. Асноўнае раўнанне для знаходжання масавага адсотка выглядае наступным чынам: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100. Малярная маса рэчыва - гэта маса аднаго молячы дадзенага рэчыва, у той час як малекулярная маса ўяўляе сабой масу аднаго молячы усяго хімічнага злучэння. Каб атрымаць працэнты, вынік дзялення памнажаецца на 100. - У пачатку рашэння задачы запішыце роўнасць: масавы працэнт = (малярная маса элемента / агульная малекулярная маса злучэння) x 100.
- Абедзве велічыні вымяраюцца ў грамах на моль (г / моль).
- Калі вам не дадзены масы, масавы адсотак якога-небудзь элемента ў зададзеным рэчыве можна знайсці, выкарыстоўваючы малярная маса.
- Прыклад 1: Знайсці масавы працэнт вадароду ў малекуле вады.
- Прыклад 2: Знайсці масавы працэнт вугляроду ў малекуле глюкозы.
 2 Запішыце хімічную формулу. Калі ў прыкладзе не дадзены хімічныя формулы зададзеных рэчываў, варта запісаць іх самастойна. Калі ж у заданні дадзены неабходныя формулы хімічных рэчываў, дадзены крок можна прапусціць і перайсці адразу да наступнага кроку (знайсці масу кожнага элемента).
2 Запішыце хімічную формулу. Калі ў прыкладзе не дадзены хімічныя формулы зададзеных рэчываў, варта запісаць іх самастойна. Калі ж у заданні дадзены неабходныя формулы хімічных рэчываў, дадзены крок можна прапусціць і перайсці адразу да наступнага кроку (знайсці масу кожнага элемента). - Прыклад 1: запішыце хімічную формулу вады, H2O.
- Прыклад 2: запішыце хімічную формулу глюкозы, C6H12O6.
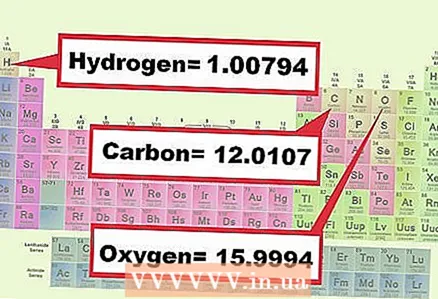 3 Знайдзіце масу кожнага элемента, якое ўваходзіць у злучэнне. Вызначыце малярны вага кожнага элемента ў хімічнай формуле па табліцы Мендзялеева. Як правіла, маса элемента паказваецца пад яго хімічным сімвалам. Выпішыце малярная маса ўсіх элементаў, якія ўваходзяць у разгляданы злучэнне.
3 Знайдзіце масу кожнага элемента, якое ўваходзіць у злучэнне. Вызначыце малярны вага кожнага элемента ў хімічнай формуле па табліцы Мендзялеева. Як правіла, маса элемента паказваецца пад яго хімічным сімвалам. Выпішыце малярная маса ўсіх элементаў, якія ўваходзяць у разгляданы злучэнне. - Прыклад 1: знайдзіце малярная маса кіслароду (15,9994) і вадароду (1,0079).
- Прыклад 2: знайдзіце малярная маса вугляроду (12,0107), кіслароду (15,9994) і вадароду (1,0079).
 4 Памножце малярная маса кожнага элемента на яго Мольн долю. Вызначце, колькі молей кожнага элемента змяшчаецца ў дадзеным хімічным рэчыве, гэта значыць Мольн долі элементаў. Мольн долі даюцца лікамі, якія стаяць у формуле ўнізе сімвалаў элементаў. Памножце малярная маса кожнага элемента на яго молярное долю.
4 Памножце малярная маса кожнага элемента на яго Мольн долю. Вызначце, колькі молей кожнага элемента змяшчаецца ў дадзеным хімічным рэчыве, гэта значыць Мольн долі элементаў. Мольн долі даюцца лікамі, якія стаяць у формуле ўнізе сімвалаў элементаў. Памножце малярная маса кожнага элемента на яго молярное долю. - Прыклад 1: пад знакам вадароду каштуе 2, а пад знакам кіслароду 1 (эквівалентна адсутнасці колькасці). Такім чынам, малярная маса вадароду варта памножыць на 2: 1,00794 X 2 = 2,01588; малярная маса кіслароду пакідаем ранейшай, 15,9994 (гэта значыць памнажаем на 1).
- Прыклад 2: пад знакам вугляроду каштуе 6, пад вадародам 12 і пад кіслародам 6. Памнажаючы малярная маса элементаў на гэтыя лікі, знаходзім:
- вуглярод: (12,0107 * 6) = 72,0642
- вадарод: (1,00794 * 12) = 12,09528
- кісларод: (15,9994 * 6) = 95,9964
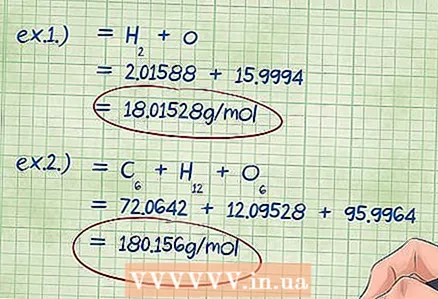 5 Вылічыце агульную масу злучэння. Складзеце знойдзеныя масы ўсіх элементаў, якія ўваходзяць у дадзенае злучэнне. Сума малярных мас элементаў, помноженных на Мольн долі, дасць вам агульную масу хімічнага злучэння. Гэты лік з'яўляецца дзельнікам ў формуле для масавага працэнта.
5 Вылічыце агульную масу злучэння. Складзеце знойдзеныя масы ўсіх элементаў, якія ўваходзяць у дадзенае злучэнне. Сума малярных мас элементаў, помноженных на Мольн долі, дасць вам агульную масу хімічнага злучэння. Гэты лік з'яўляецца дзельнікам ў формуле для масавага працэнта. - Прыклад 1: патрэбна дадаць да 2,01588 г / моль (маса двух молей атамаў вадароду) 15,9994 г / моль (маса аднаго молячы атамаў кіслароду), у выніку ў вас атрымаецца 18,01528 г / моль.
- Прыклад 2: складзеце знойдзеныя малярная маса: вуглярод + вадарод + кісларод = 72,0642 + 12,09528 + 95,9964 = 180,156 г / моль.
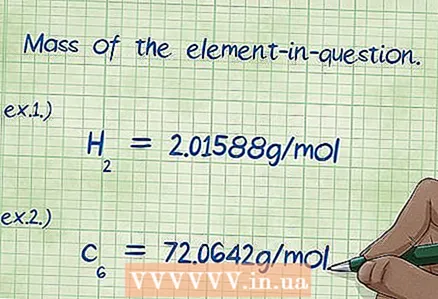 6 Вызначце масу цікавіць вас элемента. Калі вас просяць знайсці "масавы працэнт", значыць, варта вылічыць масу пэўнага элемента, якое ўваходзіць у склад злучэння, як працэнтную долю ад агульнай масы ўсіх элементаў. Знайдзіце масу зададзенага элемента і запішыце яе. Для гэтага неабходна памножыць малярная маса элемента на яго Мольн долю. У выніку ў вас атрымаецца велічыня, якая стаіць у лічніку формулы для масавага працэнта.
6 Вызначце масу цікавіць вас элемента. Калі вас просяць знайсці "масавы працэнт", значыць, варта вылічыць масу пэўнага элемента, якое ўваходзіць у склад злучэння, як працэнтную долю ад агульнай масы ўсіх элементаў. Знайдзіце масу зададзенага элемента і запішыце яе. Для гэтага неабходна памножыць малярная маса элемента на яго Мольн долю. У выніку ў вас атрымаецца велічыня, якая стаіць у лічніку формулы для масавага працэнта. - Прыклад 1: маса вадароду ў злучэнні складае 2,01588 г / моль (маса двух молей атамаў вадароду).
- Прыклад 2: маса вугляроду ў злучэнні складае 72,0642 г / моль (маса шасці молей атамаў вугляроду).
 7 Падстаўце ў раўнанне для масавага адсотка лікавыя значэнні. Пасля таго, як вы вызначыце значэнні ўсіх велічынь, падстаўце іх у формулу, якая была прыведзена на першым кроку: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100.
7 Падстаўце ў раўнанне для масавага адсотка лікавыя значэнні. Пасля таго, як вы вызначыце значэнні ўсіх велічынь, падстаўце іх у формулу, якая была прыведзена на першым кроку: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100. - Прыклад 1: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100 = (2,01588 / 18,01528) x 100.
- Прыклад 2: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100 = (72,0642 / 180,156) x 100.
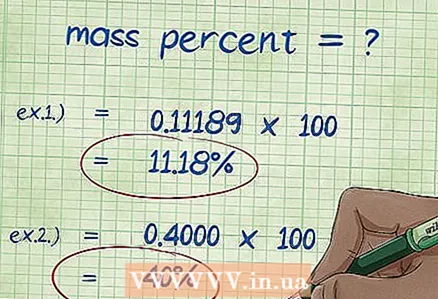 8 Вылічыце масавы працэнт. Пасля падстаноўкі лікавых значэнняў выканайце неабходныя арыфметычныя дзеянні.Падзяліце масу элемента на агульную масу злучэння і памножце на 100. У выніку ў вас атрымаецца масавы адсотак элемента.
8 Вылічыце масавы працэнт. Пасля падстаноўкі лікавых значэнняў выканайце неабходныя арыфметычныя дзеянні.Падзяліце масу элемента на агульную масу злучэння і памножце на 100. У выніку ў вас атрымаецца масавы адсотак элемента. - Прыклад 1: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100 = (2,01588 / 18,01528) x 100 = 0,11189 x 100 = 11,18%. Такім чынам, масавы адсотак атамаў вадароду ў малекуле вады роўны 11,18%.
- Прыклад 2: масавы адсотак = (малярная маса элемента / агульная малекулярная маса злучэння) x 100 = (72,0642 / 180,156) x 100 = 0,4000 x 100 = 40,00%. Такім чынам, масавы адсотак атамаў вугляроду ў малекуле глюкозы складае 40,00%.



