Аўтар:
Frank Hunt
Дата Стварэння:
16 Марш 2021
Дата Абнаўлення:
1 Ліпень 2024

Задаволены
- Крок
- Спосаб 1 з 2: Выкарыстанне хуткіх правілаў
- Спосаб 2 з 2: Разлік растваральнасці К.сп
- Неабходнасці
- Парады
- Папярэджанні
У хіміі растваральнасць выкарыстоўваецца для апісання ўласцівасцей цвёрдага рэчыва, якое змешваецца і цалкам раствараецца ў вадкасці, не пакідаючы нераствараных часціц. Раствараюцца толькі (зараджаныя) іённыя злучэнні. Для практычных мэтаў дастаткова запомніць некалькі правілаў альбо пракансультавацца са спісам правілаў, каб даведацца, ці застанецца большасць іённых злучэнняў цвёрдымі пры змешванні з вадой, альбо значная колькасць растворыцца. У рэчаіснасці некаторыя малекулы раствараюцца, нават калі вы не бачыце якіх-небудзь змен, таму для дакладных эксперыментаў вам трэба будзе ведаць, як вылічыць гэтую колькасць.
Крок
Спосаб 1 з 2: Выкарыстанне хуткіх правілаў
 Даведайцеся больш пра іённыя злучэнні. У кожным атаме звычайна ёсць колькасць электронаў, але часам яны атрымліваюць альбо губляюць адзін лішні электрон. Вынік адзін іённы з электрычным зарадам. Калі іён з адмоўным зарадам (дадатковы электрон) сустракаецца з іёнам са станоўчым зарадам (электрон адсутнічае), яны звязваюцца, як і адмоўны і станоўчы канцы двух магнітаў. У выніку атрымліваецца іённая сувязь.
Даведайцеся больш пра іённыя злучэнні. У кожным атаме звычайна ёсць колькасць электронаў, але часам яны атрымліваюць альбо губляюць адзін лішні электрон. Вынік адзін іённы з электрычным зарадам. Калі іён з адмоўным зарадам (дадатковы электрон) сустракаецца з іёнам са станоўчым зарадам (электрон адсутнічае), яны звязваюцца, як і адмоўны і станоўчы канцы двух магнітаў. У выніку атрымліваецца іённая сувязь. - Іёны з адмоўным зарадам называюцца аніёны, і іёны з станоўчым зарадам катыёны.
- Звычайна колькасць электронаў у атаме роўна колькасці пратонаў, дзе электрычныя зарады знаходзяцца ў раўнавазе.
 Ведаць растваральнасць. Малекулы вады (H.2О) маюць незвычайную структуру, з якой яны паводзяць сябе як магніт: адзін канец мае станоўчы зарад, а другі канец зараджаны адмоўна. Калі вы змешваеце іённую сувязь з вадой, гэтыя "вадзяныя магніты" будуць збірацца вакол яе, спрабуючы разабраць станоўчыя і адмоўныя іёны. Некаторыя іённыя сувязі не вельмі цесныя паміж сабой; гэтыя растваральнытаму што вада разарве і растворыць сувязь. Іншыя кампазіты маюць больш трывалыя сувязі і ёсць Не вырашаеццатаму што яны могуць зліпацца, нягледзячы на малекулы вады.
Ведаць растваральнасць. Малекулы вады (H.2О) маюць незвычайную структуру, з якой яны паводзяць сябе як магніт: адзін канец мае станоўчы зарад, а другі канец зараджаны адмоўна. Калі вы змешваеце іённую сувязь з вадой, гэтыя "вадзяныя магніты" будуць збірацца вакол яе, спрабуючы разабраць станоўчыя і адмоўныя іёны. Некаторыя іённыя сувязі не вельмі цесныя паміж сабой; гэтыя растваральнытаму што вада разарве і растворыць сувязь. Іншыя кампазіты маюць больш трывалыя сувязі і ёсць Не вырашаеццатаму што яны могуць зліпацца, нягледзячы на малекулы вады. - Некаторыя злучэнні маюць унутраныя сувязі, супастаўныя па трываласці з цягам вады. Гэтыя рэчывы ёсць умерана раствараецца, таму што значная частка (але не ўсе) аблігацый будзе разабрана.
 Вывучыце правілы растваральнасці. Паколькі ўзаемадзеянне паміж атамамі даволі складанае, не заўсёды інтуітыўна зразумела, якія злучэнні растваральныя і нерастваральныя. Знайдзіце першы іён у злучэнні ў спісе ніжэй, каб даведацца, як ён звычайна сябе паводзіць, а затым праверце выключэнні, каб пераканацца, што другі іён не ўзаемадзейнічае ненармальна.
Вывучыце правілы растваральнасці. Паколькі ўзаемадзеянне паміж атамамі даволі складанае, не заўсёды інтуітыўна зразумела, якія злучэнні растваральныя і нерастваральныя. Знайдзіце першы іён у злучэнні ў спісе ніжэй, каб даведацца, як ён звычайна сябе паводзіць, а затым праверце выключэнні, каб пераканацца, што другі іён не ўзаемадзейнічае ненармальна. - Напрыклад, выкарыстоўваць хларыд стронцыю (SrCl2), знайдзіце Sr або Cl тоўстымі крокамі, указанымі ніжэй. Cl "у асноўным вырашальны", таму праверце выключэнні ніжэй. Sr не пазначана як выключэнне, таму SrCl2 быць растваральным.
- Самыя распаўсюджаныя выключэнні з кожнага правіла пералічаны ніжэй. Ёсць і іншыя выключэнні, але вы, верагодна, не знойдзеце іх у звычайным класе хіміі альбо ў лабараторыі.
 Злучэнні раствараюцца, калі ўтрымліваюць шчолачныя металы, у тым ліку Li, Na, K, Rb і Cs. Іх таксама называюць элементамі групы IA: літый, натрый, калій, рубідый і цэзій. Амаль любое злучэнне з любым з гэтых іёнаў раствараецца.
Злучэнні раствараюцца, калі ўтрымліваюць шчолачныя металы, у тым ліку Li, Na, K, Rb і Cs. Іх таксама называюць элементамі групы IA: літый, натрый, калій, рубідый і цэзій. Амаль любое злучэнне з любым з гэтых іёнаў раствараецца. - Выключэнне: Лі3PO4 не раствараецца.
 Злучэння з NO3, З2Х.3О2, НЕ2, ClO3 і ClO4 растваральныя. Гэта іёны нітратаў, ацэтатаў, нітрытаў, хлоратаў і перхларатаў. Звярніце ўвагу, што ацэтат часта скарачаюць з OAc.
Злучэння з NO3, З2Х.3О2, НЕ2, ClO3 і ClO4 растваральныя. Гэта іёны нітратаў, ацэтатаў, нітрытаў, хлоратаў і перхларатаў. Звярніце ўвагу, што ацэтат часта скарачаюць з OAc. - Выключэнні: Ag (OAc) (ацэтат срэбра) і Hg (OAc)2 (ацэтат ртуці) не раствараецца.
- AgNO2 і KClO4 з'яўляюцца толькі "часткова растваральнымі".
 злучэнні з Cl, Br і I звычайна растваральныя. Іёны хларыдаў, брамідаў і ёдыдаў амаль заўсёды ўтвараюць растваральныя злучэнні, якія таксама называюць галогенавымі солямі.
злучэнні з Cl, Br і I звычайна растваральныя. Іёны хларыдаў, брамідаў і ёдыдаў амаль заўсёды ўтвараюць растваральныя злучэнні, якія таксама называюць галогенавымі солямі. - Выключэнне: Калі што-небудзь з гэтага звязваецца з іёнамі срэбра (Ag), ртуць (Hg2), альбо свінец (Pb), вынік не раствараецца. Тое ж датычыцца і менш распаўсюджаных злучэнняў з меддзю (Cu) і таліем (Tl).
 Злучэння з SO4 звычайна растваральныя. Сульфатна-іённы звычайна ўтварае растваральныя злучэнні, але ёсць некалькі выключэнняў.
Злучэння з SO4 звычайна растваральныя. Сульфатна-іённы звычайна ўтварае растваральныя злучэнні, але ёсць некалькі выключэнняў. - Выключэнні: Іён сульфату ўтварае нерастваральныя злучэнні з наступнымі іёнамі: стронцый Sr, барый Ba, свінец Pb, срэбра Ag, кальцый Ca, радый Ra і двухатамнае срэбра Ag2. Звярніце ўвагу, што сульфат срэбра і сульфат кальцыя раствараюцца роўна столькі, каб іх часам называлі цяжка растваральнымі.
 Злучэння з OH або S не раствараюцца. Гэта іёны гідраксіду і сульфіду адпаведна.
Злучэння з OH або S не раствараюцца. Гэта іёны гідраксіду і сульфіду адпаведна. - Выключэнні: Вы памятаеце шчолачныя металы (група I-A) і наколькі яны любяць утвараць нерастваральныя злучэнні? Усе Li, Na, K, Rb і Cs ўтвараюць растваральныя злучэнні з іёнамі гідраксіду або сульфіду. Акрамя таго, гідраксід утварае растваральныя солі з іёнамі шчолачназямельных металаў (ІІ-А групы): кальцыя Са, стронцыю Sr і барыю Ва. Звярніце ўвагу, што гідраксід з шчолачна-зямельным злучэннем мае дастаткова малекул, каб склейвацца, і часам іх можна лічыць "маларастваральнымі".
 Злучэння з СА3 альбо PO4 не раствараюцца. У апошні раз праверце наяўнасць іёнаў карбанату і фасфатаў, і вы павінны ведаць, чаго чакаць ад злучэння.
Злучэння з СА3 альбо PO4 не раствараюцца. У апошні раз праверце наяўнасць іёнаў карбанату і фасфатаў, і вы павінны ведаць, чаго чакаць ад злучэння. - Выключэнні: Гэтыя іёны ўтвараюць растваральныя злучэнні са звычайнымі рэчывамі, шчолачнымі металамі Li, Na, K, Rb і Cs, а таксама з амоніям NH4.
Спосаб 2 з 2: Разлік растваральнасці К.сп
 Знайдзіце прадукт растваральнасці канстанты К.сп. Гэтая канстанта адрозніваецца для кожнага злучэння, таму вам трэба будзе знайсці яе ў табліцы ў падручніку альбо ў Інтэрнэце. Паколькі гэтыя значэнні вызначаюцца эксперыментальна, яны могуць моцна адрознівацца ад табліцы да табліцы, таму лепш выкарыстоўваць табліцу ў падручніку, калі яна ёсць. Калі не пазначана іншае, у большасці табліц тэмпература навакольнага асяроддзя складае 25 ° С.
Знайдзіце прадукт растваральнасці канстанты К.сп. Гэтая канстанта адрозніваецца для кожнага злучэння, таму вам трэба будзе знайсці яе ў табліцы ў падручніку альбо ў Інтэрнэце. Паколькі гэтыя значэнні вызначаюцца эксперыментальна, яны могуць моцна адрознівацца ад табліцы да табліцы, таму лепш выкарыстоўваць табліцу ў падручніку, калі яна ёсць. Калі не пазначана іншае, у большасці табліц тэмпература навакольнага асяроддзя складае 25 ° С. - Напрыклад, калі вы хочаце растварыць ёдыд свінцу (PbI2), запішыце канстанту раўнавагі прадукту растваральнасці. Калі вы выкарыстоўваеце табліцу на bilbo.chm.uri.edu, выкарыстоўвайце канстанту 7,1 × 10.
 Спачатку запішыце хімічнае ўраўненне. Спачатку вызначыце, як злучэнне распадаецца на іёны пры растварэнні. Цяпер напішыце ўраўненне з К.сп з аднаго боку, і асобныя іёны, з іншага.
Спачатку запішыце хімічнае ўраўненне. Спачатку вызначыце, як злучэнне распадаецца на іёны пры растварэнні. Цяпер напішыце ўраўненне з К.сп з аднаго боку, і асобныя іёны, з іншага. - Напрыклад, малекула PbI2 распадаецца на іёны Pb, I і іншае I (вам трэба толькі ведаць або шукаць зарад аднаго іона, бо вы ведаеце, што агульнае злучэнне заўсёды мае нейтральны зарад).
- Запішыце ўраўненне 7,1 × 10 = [Pb] [I]
 Наладзьце ўраўненне, каб выкарыстоўваць зменныя. Перапішыце ўраўненне як адзіную задачу алгебры, выкарыстоўваючы свае веды пра колькасць малекул ці іёнаў. Усталюйце x роўным колькасці рэчыва, якое растварыцца, і перапішыце зменныя як нумары кожнага іёна праз x.
Наладзьце ўраўненне, каб выкарыстоўваць зменныя. Перапішыце ўраўненне як адзіную задачу алгебры, выкарыстоўваючы свае веды пра колькасць малекул ці іёнаў. Усталюйце x роўным колькасці рэчыва, якое растварыцца, і перапішыце зменныя як нумары кожнага іёна праз x. - У нашым прыкладзе мы перапісваем 7,1 × 10 = [Pb] [I]
- Паколькі ў злучэнні толькі адзін іён свінцу (Pb), колькасць раствораных малекул злучэння будзе роўна колькасці свабодных іёнаў свінцу. Такім чынам, мы можам замяніць [Pb] на x.
- Паколькі на кожны іён свінцу прыпадае два іёны ёду (I), мы можам прыраўнаваць колькасць атамаў ёду да 2х.
- Ураўненне цяпер выглядае 7,1 × 10 = (x) (2x)
 Разгледзім агульныя іёны, калі такія маюцца. Прапусціце гэты крок, калі вы раствараеце злучэнне ў чыстай вадзе. Аднак калі злучэнне раствараецца ў растворы, які ўжо ўтрымлівае адзін або некалькі ўваходзяць у склад іёнаў ("агульны іён"), растваральнасць значна зніжаецца. Эфект агульных іёнаў найбольш прыкметны ў злучэннях, якія ў асноўным нерастваральныя, і ў гэтых выпадках можна меркаваць, што пераважная большасць іёнаў у раўнавазе паходзіць ад іона, ужо прысутнага ў растворы. Перапішыце ўраўненне з вядомай малярнай канцэнтрацыяй (моляў на літр, або М) іёнаў, якія ўжо знаходзяцца ў растворы, замяніўшы значэнне х, якое вы выкарыстоўвалі для гэтага іёна.
Разгледзім агульныя іёны, калі такія маюцца. Прапусціце гэты крок, калі вы раствараеце злучэнне ў чыстай вадзе. Аднак калі злучэнне раствараецца ў растворы, які ўжо ўтрымлівае адзін або некалькі ўваходзяць у склад іёнаў ("агульны іён"), растваральнасць значна зніжаецца. Эфект агульных іёнаў найбольш прыкметны ў злучэннях, якія ў асноўным нерастваральныя, і ў гэтых выпадках можна меркаваць, што пераважная большасць іёнаў у раўнавазе паходзіць ад іона, ужо прысутнага ў растворы. Перапішыце ўраўненне з вядомай малярнай канцэнтрацыяй (моляў на літр, або М) іёнаў, якія ўжо знаходзяцца ў растворы, замяніўшы значэнне х, якое вы выкарыстоўвалі для гэтага іёна. - Напрыклад, калі наша злучэнне ёду-свінцу растварылі ў растворы, які змяшчае 0,2 М хларыду свінцу (PbCl2), то мы можам перапісаць ураўненне ў выглядзе 7,1 × 10 = (0,2M + x) (2x). А потым, паколькі 0,2M - гэта больш высокая канцэнтрацыя, чым x, мы можам смела перапісаць гэта як 7,1 × 10 = (0,2M) (2x).
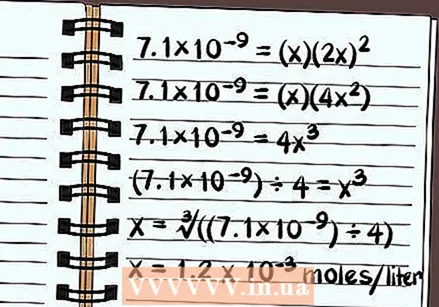 Рашы ўраўненне. Рашыце на х і даведайцеся, наколькі злучэнне раствараецца. З-за спосабу вызначэння канстанты растваральнасці ваш адказ будзе выказаны як колькасць моляў растворанага злучэння на літр вады. Каб знайсці канчатковы адказ, вам можа спатрэбіцца калькулятар.
Рашы ўраўненне. Рашыце на х і даведайцеся, наколькі злучэнне раствараецца. З-за спосабу вызначэння канстанты растваральнасці ваш адказ будзе выказаны як колькасць моляў растворанага злучэння на літр вады. Каб знайсці канчатковы адказ, вам можа спатрэбіцца калькулятар. - Далейшае тычыцца растваральнасці ў чыстай вадзе, а не ў звычайных іёнах.
- 7,1 × 10 = (x) (2x)
- 7,1 × 10 = (х) (4x)
- 7,1 × 10 = 4x
- (7,1 × 10) ÷ 4 = х
- x = ∛ ((7,1 × 10) ÷ 4)
- х = 1,2 х 10 моляў на літр раствараецца. Гэта вельмі малая колькасць, таму вы ведаеце, што гэта злучэнне ў прынцыпе дрэнна раствараецца.
Неабходнасці
- Табліца канстант прадуктаў растваральнасці (К.сп) для злучэнняў.
Парады
- Калі ў вас ёсць дадзеныя эксперыментаў пра ступень растварэння злучэння, вы можаце выкарыстоўваць тое ж самае ўраўненне для вырашэння канстанты растваральнасці Kсп.
Папярэджанні
- Агульнапрынятага вызначэння гэтых тэрмінаў няма, але хімікі сыходзяцца ў меркаванні наконт большасці злучэнняў. Некаторыя маргінальныя выпадкі, якія тычацца злучэнняў са значнай доляй раствораных і нераствараных малекул, можна апісаць з дапамогай розных табліц растваральнасці.
- Некаторыя старыя падручнікі даюць NH4OH зноў як растваральны склад. Гэта няправільна; невялікая колькасць NH4 і іёны ОН можна назіраць, але іх нельга вылучыць, утвараючы злучэнне.



