Аўтар:
John Stephens
Дата Стварэння:
1 Студзень 2021
Дата Абнаўлення:
29 Чэрвень 2024

Задаволены
Вы калі-небудзь пакідалі бутэльку вады на сонцы на некалькі гадзін, потым адчынялі крышку і чулі маленькі "поп"? Гэты гук належны ціск пары у бутэльцы прычыны. У хіміі ціск пары - гэта ціск, які дзейнічае на сценку закрытай пасудзіны, калі вадкасць у пасудзіне выпараецца (ператвараецца ў газ). Каб знайсці ціск пары пры вядомай тэмпературы, выкарыстоўвайце ўраўненне Клаўзіуса-Клапейрона: ln (P1 / P2) = (ΔHвап/ R) ((1 / T2) - (1 / T1)).
Крокі
Спосаб 1 з 3: Выкарыстоўвайце ўраўненне Клаўзія-Клапейрона
Напішыце ўраўненне Клаўзія-Клапейрона. Пры разглядзе змены ціску пары з цягам часу формулай вылічэння ціску пары з'яўляецца ўраўненне Клаўзія-Клапейрона (названа ў гонар фізікаў Рудольфа Клаўзіуса і Бенуа Поля Эміля Клапейрона). Гэта часта выкарыстоўваная формула для вырашэння агульных праблем ціску пара ў фізіцы і хіміі. Формула пішацца наступным чынам: ln (P1 / P2) = (ΔHвап/ R) ((1 / T2) - (1 / T1)). У гэтай формуле зменныя ўяўляюць: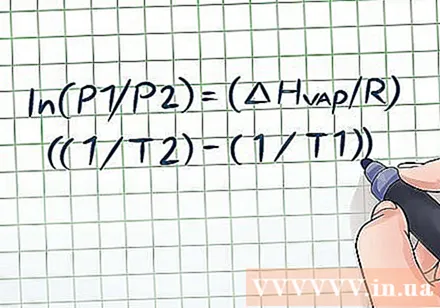
- ΔHвап: Энтальпія выпарэння вадкасцей. Гэта значэнне можна знайсці ў табліцы ў канцы падручніка па хіміі.
- R: Ідэальная газавая пастаянная і роўная 8314 Дж / (K × моль).
- T1: Тэмпература, пры якой вядомы ціск пары (пачатковая тэмпература).
- T2: Тэмпература, пры якой неабходны ціск пары (канчатковая тэмпература).
- Р1 і Р2: Адпаведны ціск пары пры тэмпературах Т1 і Т2.
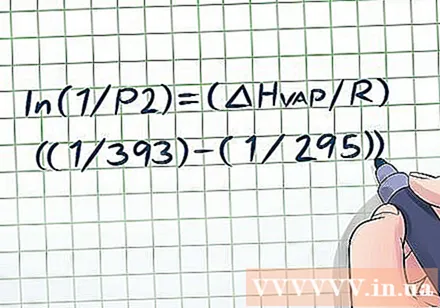
Падстаўце вядомыя значэнні зменным. Ураўненне Клаўзіуса-Клапейрона выглядае досыць складана, паколькі існуе мноства розных зменных, але гэта не занадта складана, калі задача дае дастаткова інфармацыі. Самыя асноўныя праблемы ціску пара дадуць вам два значэнні тэмпературы і адно значэнне ціску альбо два значэнні ціску і адно значэнне тэмпературы - як толькі вы атрымаеце гэтыя дадзеныя, гэта лёгка вырашыць.- Напрыклад, выкажам здагадку, што праблема складаецца ў ёмістасці з вадкасцю пры 295 К і ціскам пары 1 атмасфера (атм). Пытанне: Які ціск пары пры тэмпературы 393 К? У нас ёсць два значэнні для тэмпературы і адно для ціску, таму для астатняга ціску можна вырашыць ураўненне Клаўзія-Клапейрона. Укладваючы значэнні ў зменныя, мы маем ln (1 / P2) = (ΔHвап/ R) ((1/393) - (1/295)).
- Для ўраўнення Клаўзіуса-Клапейрона мы заўсёды павінны выкарыстоўваць значэнне тэмпературы Кельвін. Вы можаце выкарыстоўваць любое значэнне ціску, пакуль яно аднолькавае для P1 і P2.
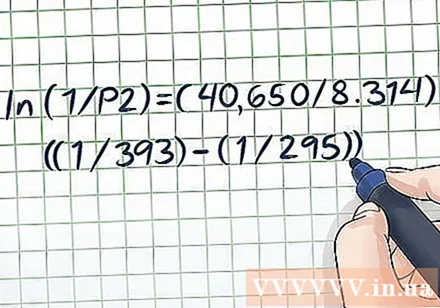
Заменіце канстанты. Ураўненне Клаўзія-Клапейрона мае дзве канстанты: R і ΔHвап. R заўсёды роўны 8314 Дж / (K × Моль). Аднак ΔHвап (лятучая энтальпія) залежыць ад тыпу выпарнай вадкасці, якая ўзнікае пры задачы. З улікам сказанага, вы можаце шукаць значэнні ΔHвап разнастайных рэчываў у канцы падручніка па хіміі ці фізіцы, альбо знайдзіце іх у Інтэрнэце (напрыклад, тут.)- У прыведзеным вышэй прыкладзе выкажам здагадку, што вадкасць ёсць чыстая вада. Калі шукаць у табліцы значэнне Hвап, маем ΔHвап вычышчанай вады складае прыблізна 40,65 кДж / моль. Паколькі ў значэнні H выкарыстоўваюцца джоўлі, мы павінны пераўтварыць яго ў 40 650 Дж / моль.
- Паставіўшы канстанты ва ўраўненне, мы маем ln (1 / P2) = (40 650/8 314) ((1/393) - (1/295)).
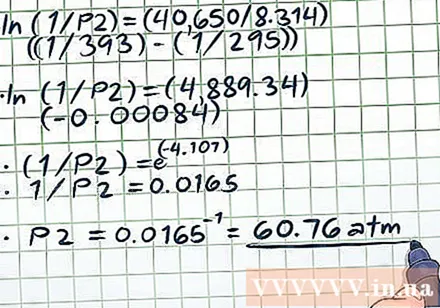
Рашы ўраўненне. Пасля таго, як вы ўставілі ўсе значэнні ў зменныя ўраўнення, акрамя зменнай, якую мы вылічваем, працягвайце рашаць ураўненне паводле звычайнага алгебраічнага прынцыпу.- Самы складаны момант пры рашэнні ўраўнення (ln (1 / P2) = (40 650/8 314) ((1/393) - (1/295))) - гэта апрацоўка натуральнай лагарыфмічнай функцыі (ln). Каб выключыць натуральную функцыю часопіса, выкарыстоўвайце абодва бакі ўраўнення ў якасці паказчыка для матэматычнай канстанты е. Іншымі словамі, ln (x) = 2 → e = e → x = e.
- Зараз разбярэм ураўненне прыкладу:
- ln (1 / P2) = (40 650/8 314) ((1/393) - (1/295))
- ln (1 / P2) = (4889,34) (- 0,00084)
- (1 / P2) = е
- 1 / Р2 = 0,0165
- Р2 = 0,0165 = 60,76 атм. Гэтая велічыня разумная - у закрытай посудзе пры павышэнні тэмпературы амаль на 100 градусаў (да тэмпературы, прыблізна на 20 градусаў вышэй за тэмпературу кіпення вады) утвараецца шмат пары, таму ціск будзе павялічвацца. шмат.
Спосаб 2 з 3: Знайдзіце ціск пары растворанага раствора
Напішыце закон Рауля. На самай справе мы рэдка працуем з чыстымі вадкасцямі - часта даводзіцца працаваць са сумесямі мноства розных рэчываў. Некаторыя звычайныя сумесі ствараюцца шляхам растварэння невялікай колькасці хімічнага рэчыва, званага раствораны у вялікай колькасці іншых хімічных рэчываў называецца Растваральнік фарміраваць раствор. У гэтым выпадку нам трэба ведаць ураўненне Закона Рауля (імя фізіка Франсуа-Мары Рауля), якое выглядае так: Праствор= РРастваральнікXРастваральнік. У гэтай формуле зменныя ўяўляюць: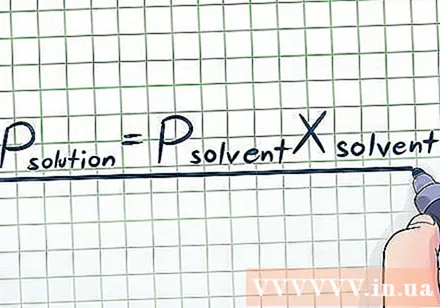
- Праствор: Ціск пары ўсяго раствора (усіх кампанентаў раствора)
- ПРастваральнік: Ціск пары растваральніка
- XРастваральнік: Малярная доля растваральніка.
- Не хвалюйцеся, калі вы яшчэ не ведаеце тэрмін "малярная частка" - мы растлумачым гэта на наступных этапах.
Адрозніваюць растваральнікі і растваральнікі ў растворы. Перш чым вылічыць ціск пары раствора, трэба вызначыць рэчывы, якія ўказваюцца задачай. Звярніце ўвагу, што раствор утвараецца пры растварэнні растваральніка ў растваральніку - раствораная хімічная рэчыва заўсёды з'яўляецца раствораным рэчывам, а хімічнае рэчыва, якое выконвае гэтую працу, з'яўляецца растваральнікам.
- У гэтым раздзеле мы возьмем просты прыклад для ілюстрацыі вышэйзгаданых паняццяў. Дапусцім, мы хочам знайсці ціск пары раствора сіропу. Звычайна сіроп рыхтуюць з адной часткі цукру, растворанай у адной частцы вады, таму і гаворым цукар з'яўляецца раствораным рэчывам, а вада - растваральнікам.
- Заўвага: хімічнай формулай цукрозы (цукровага пяску) з'яўляецца C12Н22О11. Вы знойдзеце гэтую інфармацыю вельмі важнай.
Знайдзіце тэмпературу раствора. Як мы бачым у згаданым вышэй раздзеле Клаўзія Клапейрона, тэмпература вадкасці будзе ўплываць на яе ціск пары. Увогуле, чым вышэй тэмпература, тым вышэй ціск пары - па меры павелічэння тэмпературы, больш вадкасці выпараецца і павялічвае ціск у пасудзіне.
- У гэтым прыкладзе выкажам здагадку, што бягучая тэмпература сіропу складае 298 Да (каля 25 С).
Знайдзіце ціск пары растваральніка. Хімічныя спасылкі звычайна даюць значэнні ціску пары для многіх распаўсюджаных рэчываў і сумесяў, але звычайна толькі для значэнняў ціску пры 25 ° C / 298 K або пры тэмпературы кіпення. Калі ў вашым растворы ёсць такая тэмпература, вы можаце выкарыстоўваць эталоннае значэнне, інакш вам трэба знайсці ціск пары пры пачатковай тэмпературы раствора.
- Тут можа дапамагчы ўраўненне Клаўзіуса-Клапейрона, якое выкарыстоўвае ціск і тэмпературу 298 K (25 C) для P1 і T1.
- У гэтым прыкладзе сумесь мае тэмпературу 25 ° C, таму мы можам выкарыстоўваць даведку. Мы бачым ваду пры тэмпературы 25 ° C з ціскам пары 23,8 мм рт
Знайдзіце малярную долю растваральніка. Апошняе, што вам трэба зрабіць перад рашэннем вынікаў, - знайсці малярную долю растваральніка. Гэта даволі проста: проста пераўтварыце інгрэдыенты ў радзімкі, а потым знайдзіце працэнт кожнага з агульных моляў сумесі. Іншымі словамі, малярная частка кожнага кампанента роўная (колькасць молей сумесі) / (агульная колькасць моляў сумесі).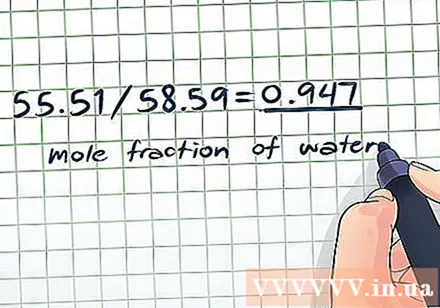
- Дапусцім, што рэцэпт сіропу ёсць 1 літр (л) вады і 1 літр цукрозы (цукар). Тады нам трэба знайсці колькасць радзімак кожнага інгрэдыента. Для гэтага мы знойдзем масы кожнага кампанента, а затым выкарыстаем малярную масу гэтых кампанентаў для выпрацоўкі радзімак.
- Вага (1 л вады): 1000 грам (г)
- Вага (1 л сырога цукру): прыблізна 10556,7 г.
- Колькасць радзімак (вада): 1000 грам × 1 моль / 18 015 г = 55,51 моль
- Радзімкі (цукар): 1056,7 грама × 1 моль / 342,2965 г = 3,08 моль (Звярніце ўвагу, што вы можаце знайсці малярную масу цукру па яго хімічнай формуле, З12Н22О11.)
- Усяго радзімкі: 55,51 + 3,08 = 58,59 радзімкі
- Малярная доля вады: 55,51 / 58,59 = 0,947
Вырашыць вынікі. Нарэшце, у нас дастаткова дадзеных для рашэння ўраўнення Рауля. Гэта вельмі проста: падключыце значэнні да зменных ураўнення тэарэмы Рауля, згаданых у пачатку гэтага раздзела (Праствор = РРастваральнікXРастваральнік).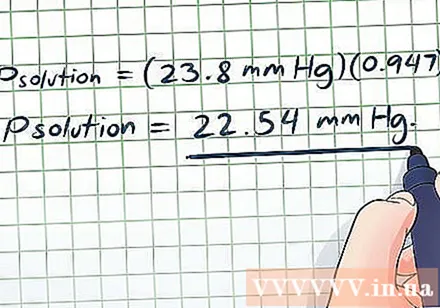
- Падставіўшы значэнні, мы маем:
- Праствор = (23,8 мм рт.сл.) (0,947)
- Праствор = 22,54 мм рт. Гэты вынік з'яўляецца разумным - у малярным выражэнні ў вялікай колькасці вады раствараецца толькі невялікая колькасць цукру (хаця гэтыя два фактычна аднолькавыя па аб'ёме), таму ціск пары толькі трохі панізіцца.
Метад 3 з 3: Знайдзіце ціск пары ў асаблівых выпадках
Вызначце стандартныя ўмовы ціску і тэмпературы. У якасці ўмоў "па змаўчанні" навукоўцы часта выкарыстоўваюць пару значэнняў ціску і тэмпературы. Гэтыя значэнні называюцца стандартным ціскам і тэмпературай (у сукупнасці называюцца стандартнымі ўмовамі або DKTC). Праблемы з ціскам пара часта спасылаюцца на DKTC, таму вы павінны запомніць гэтыя значэнні для зручнасці. DKTC вызначаецца як:
- Тэмпература: 273,15 К / 0 С / 32 Ж
- Ціск: 760 мм рт / 1 атм / 101 325 кілапаскаляў
Перайдзіце да ўраўнення Клаўзіуса-Клапейрона, каб знайсці іншыя зменныя. У прыкладзе з часткі 1 мы бачым, што ўраўненне Клаўзія-Клапейрона вельмі эфектыўна пры разліку ціску пары чыстых рэчываў. Аднак не ўсе праблемы патрабуюць пошуку P1 або P2, але шмат разоў яны нават просяць знайсці тэмпературу ці нават значэнне ΔH.вап. У гэтым выпадку, каб знайсці адказ, вам проста трэба пераключыць ураўненне так, каб патрэбная зменная знаходзілася на адным баку ўраўнення, а ўсе астатнія - на другім баку.
- Напрыклад, выкажам здагадку, што існуе невядомая вадкасць з ціскам пары 25 тор пры 273 К і 150 тор пры 325 Да, і мы хочам знайсці лятучую энтальпію гэтай вадкасці (ΔHвап). Мы можам вырашыць наступнае:
- ln (P1 / P2) = (ΔHвап/ R) ((1 / T2) - (1 / T1))
- (ln (P1 / P2)) / ((1 / T2) - (1 / T1)) = (ΔHвап/ R)
- R × (ln (P1 / P2)) / ((1 / T2) - (1 / T1)) = ΔHвап. Зараз заменім значэнні:
- 8 314 Дж / (K × Моль) × (-1,79) / (- 0,00059) = ΔHвап
- 8314 Дж / (K × Моль) × 3033,90 = ΔHвап = 25 223,83 Дж / моль
Улічыце ціск пары растворанага рэчыва пры яго выпарэнні. У прыведзеным вышэй прыкладзе закона Рауля наша раствораная маса - цукар, таму яна не выпараецца самастойна пры пакаёвай тэмпературы (думаеце, вы калі-небудзь бачылі, як міска цукру выпараецца?). Аднак калі рэчыва раствараецца сапраўды Калі ён выпарыцца, гэта адаб'ецца на агульным ціску пары раствора. Мы разлічваем гэты ціск, выкарыстоўваючы зменнае ўраўненне закона Рауля: Праствор = Σ (РінгрэдыентXінгрэдыент). Сімвал (Σ) азначае, што нам трэба скласці ўсе ціскі пары розных кампанентаў, каб знайсці адказ.
- Напрыклад, скажам, мы маем рашэнне, якое складаецца з двух хімічных рэчываў: бензолу і талуолу. Агульны аб'ём раствора складае 120 мл; 60 мл бензолу і 60 мл талуолу. Тэмпература раствора складае 25 ° С, а ціск пары кожнага хімічнага кампанента пры 25 ° С складае 95,1 мм рт.сл. для бензолу і 28,4 мм.рт.ст. для талуолу. Для зададзеных значэнняў знайдзіце ціск пары раствора. Мы можам вырашыць праблему, выкарыстоўваючы шчыльнасць, малярную масу і ціск пары двух хімічных рэчываў:
- Аб'ём (бензолу): 60 мл = 0,06 л × 876,50 кг / 1000 л = 0,053 кг = 53 г.
- Вага (талуол): 0,06 л × 866,90 кг / 1000 л = 0,052 кг = 52 г.
- Колькасць радзімак (бензол): 53 г × 1 моль / 78,11 г = 0,679 моль
- Колькасць радзімак (талуол): 52 г × 1 моль / 92,14 г = 0,564 моль
- Усяго радзімкі: 0,679 + 0,564 = 1,243
- Малярная доля (бензол): 0,679 / 1,223 = 0,546
- Малярная доля (талуол): 0,564 / 1,243 = 0,454
- Вырашыць вынікі: Pраствор = РбензолXбензол + РталуенXталуен
- Праствор = (95,1 мм рт.сл.) (0,546) + (28,4 мм рт.сл.) (0,454)
- Праствор = 51,92 мм рт.сл. + 12,89 мм рт.сл. 64,81 мм рт
Парада
- Каб выкарыстоўваць ураўненне Клаўзія Клапейрона вышэй, неабходна перавесці тэмпературу ў адзінкі Кевіна (пазначаецца K). Калі ў вас тэмпература ў Цэльсіі, зменіце яе з дапамогай наступнай формулы: Т.к = 273 + Тc
- Вы можаце ўжыць вышэйапісаныя спосабы, паколькі энергія прапарцыйная колькасці пададзенага цяпла. Тэмпература вадкасці - адзіны фактар навакольнага асяроддзя, які ўплывае на ціск пары.