Аўтар:
Monica Porter
Дата Стварэння:
22 Марш 2021
Дата Абнаўлення:
1 Ліпень 2024

Задаволены
Масавы працэнт паказвае працэнт кожнага элемента ў хімічным злучэнні. Каб знайсці адсоткавыя масы, трэба ведаць малярную масу элементаў злучэння ў грамах / моль альбо колькасць грам рэчываў, якія ўваходзяць у склад раствора. Масавы працэнт вылічваецца з дапамогай простай формулы, якая дзеліць масу элемента (альбо растворанага рэчыва) на масу злучэння (альбо раствора).
Крокі
Спосаб 1 з 2: Вылічыце працэнт масы, ведаючы масу
Вызначце ўраўненне працэнта масы ў сумесі. Асноўная формула для разліку працэнта масы ў сумесі: працэнт масы = (маса якасці / змешаная маса) х 100. Нарэшце, вы павінны памножыць на 100, каб прадставіць працэнтнае значэнне.
- Напішыце ўраўненне, пачынаючы рашаць задачу: масавы працэнт = (маса рэчыва / змешаная маса) х 100.
- Колькасць якасці будзе ўказана ў задачы. Калі тэма не прыведзена, звярніцеся да наступнага раздзела пра тое, як знайсці працэнты масы, не ведаючы ваг.
- Маса сумесі роўная агульнай масе рэчываў, якія ўваходзяць у склад сумесі ці раствора.

Разлічыце масу сумесі. Пасля таго, як вы даведаецеся масу элементаў альбо злучэнняў, усё, што вам трэба зрабіць, гэта скласці іх, каб атрымаць масу канчатковай сумесі ці раствора. Гэта назоўнік у формуле працэнтнай масы.- Прыклад 1: Які масавы працэнт складае 5 г гідраксіду натрыю пры растварэнні ў 100 г вады?
- Маса сумесі - агульная маса гідраксіду натрыю і вады: 100 г + 5 г. Такім чынам, змяшаная вага складае 105 г.
- Прыклад 2: Якая маса хларыду натрыю і вады патрэбна для адукацыі 175 г 15% раствора?
- У гэтым прыкладзе, дзе вы ведаеце змешаную масу і працэнт масы, заданне просіць знайсці колькасць дададзенай растворанай рэчывы. Маса сумесі - 175 г.
- Прыклад 1: Які масавы працэнт складае 5 г гідраксіду натрыю пры растварэнні ў 100 г вады?

Вызначце масу рэчыва, каб знайсці працэнтную масу. Калі віктарына просіць знайсці "працэнт масы" рэчыва, вы павінны знайсці масу рэчыва ў працэнтах ад агульнай масы ўсіх інгрэдыентаў. Запішыце масу рэчыва, каб знайсці працэнтную масу. Гэта лічнік у формуле працэнтнай масы.- Прыклад 1: Маса гідраксіду натрыю (рэчыва, якое можна знайсці па масавай долі) складае 5 г.
- Прыклад 2: У гэтым прыкладзе колькасць рэчыва шукае працэнт невядомай масы, а вы яго шукаеце.

Заменіце зменныя раўнаннем масавых працэнтаў. Пасля таго, як вы вызначылі значэнне кожнай зменнай, проста падключыце іх да ўраўнення.- Прыклад 1: масавы працэнт = (маса рэчыва / змешаная маса) х 100 = (5 г / 105 г) х 100.
- Прыклад 2: Нам трэба пераўтварыць ураўненне працэнта масы, каб вылічыць колькасць невядомай якасці: маса якасці = (працэнт масы * змешаная маса) / 100 = (15 * 175) / 100 .
Вылічыце працэнт аб'ёму. Цяпер, калі ўраўненне запоўнена, вам трэба толькі вылічыць працэнт масы. Падзяліце масу рэчыва на масу сумесі, затым памножце на 100. Гэта масавы працэнт рэчыва ў сумесі.
- Прыклад 1: (5/105) х 100 = 0,04761 х 100 = 4,761%. Такім чынам, масавы працэнт 5 г гідраксіду натрыю, растворанага ў 100 г вады, складае 4761%.
- Прыклад 2: Ураўненне пасля пераўтварэння для вылічэння колькасці якасці складае (працэнтная маса * змешаны вага) / 100: (15 * 175) / 100 = (2625) / 100 = 26,25 грама хлорысты натрый.
- Вага дададзенай вады - гэта маса сумесі, мінус вага рэчыва: 175 - 26,25 = 148,75 грама вады.
Спосаб 2 з 2: Вылічыце працэнт масы, калі маса невядомая
Вызначце ўраўненне працэнта масы ў злучэнні. Асноўная формула працэнта масы ў злучэнні: масавы працэнт = (малярная малярная маса / малярная маса злучэння) х 100. Элементальная малярная маса - гэта маса аднаго моля элемента у той час як малекулярная маса - гэта маса аднаго моля злучэння. Нарэшце, вы павінны памножыць на 100, каб атрымаць працэнтнае значэнне.
- Напішыце ўраўненне, пачынаючы рашаць задачу: масавы працэнт = (элементарная малярная маса / малярная маса злучэння) х 100.
- Адзінкамі двух вышэйзгаданых значэнняў з'яўляюцца грамы на моль (г / моль).
- Калі задача не дае масы, вы можаце выкарыстоўваць малярную масу, каб вылічыць працэнт масы элемента.
- Прыклад 1: Вылічыце масавы працэнт вадароду ў малекуле вады.
- Прыклад 2: Разлічыце масавы працэнт вугляроду ў малекуле глюкозы.
Пішыце Хімічная формула. Калі праблема не ахоплівае хімічныя формулы для кожнага злучэння, вам трэба будзе запісаць іх. Калі праблема заключаецца ў хімічнай формуле, прапусціце гэты этап і перайдзіце да этапу "Знайсці масу кожнага элемента".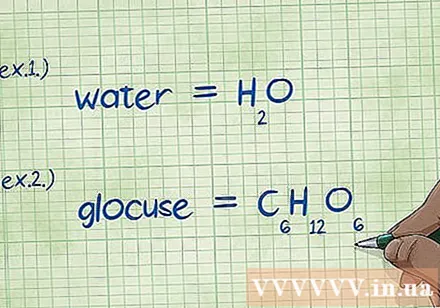
- Прыклад 1: Напішыце хімічную формулу вады H2О.
- Прыклад 2: Напішыце хімічную формулу глюкозы, З6Н12О6.
Знайдзіце масу кожнага элемента ў злучэнні. Знайдзіце малекулярную масу кожнага элемента ў хімічнай формуле ў перыядычнай табліцы. Маса элементаў звычайна пішацца пад хімічным сімвалам. Запішыце масу кожнага элемента ў злучэнні.
- Прыклад 1: Мы можам выявіць, што масавы атам кіслароду складае 159999; а кубічны атам вадароду - 10079.
- Прыклад 2: Мы выявілі, што масавы атам вугляроду складае 120107; кісларод - 15 9994; а вадарод - 1,0079.
Памножце кубічны атам на малярнае суадносіны. Вызначце колькасць радзімак (мольнае суадносіны) кожнага элемента ў хімічным злучэнні. Малярнае суадносіны вылічаецца па невялікай колькасці, прыведзенай ніжэй у хімічнай формуле злучэння. Памножце кубічны атам кожнага элемента на малярнае суадносіны.
- Прыклад 1: вадарод мае два індэксы, а кісларод - 1. Так памножце малекулярную масу вадароду на 2, 100794 X 2 = 201588; а малекулярная маса кіслароду - 15 9994 (памножаная на адзінку).
- Прыклад 2: вуглярод мае індэкс 6, вадарод - 12, кісларод - 6. Памножце кубічны атам кожнага элемента на паказчык ніжэй.
- Вуглярод (120107 * 6) = 72 064
- Вадарод (100794 * 12) = 12 09528
- Кісларод (159999 * 6) = 95,9964
Вылічыце агульную масу злучэння. Дадайце масы ўсіх элементаў злучэння. Вы можаце вылічыць агульную масу злучэнняў, выкарыстоўваючы масы, выражаныя ў малярных суадносінах. Гэты лік будзе назоўнікам ва ўраўненні працэнтнай масы.
- Прыклад 1: Даданне 201588 г / моль (маса двух моляў атамаў вадароду) да 159999 г / моль (маса аднаго моля атамаў кіслароду) дае 181528 г / моль.
- Прыклад 2: Складзіце ўсе вагі разам: вуглярод + вадарод + кісларод = 72,0642 + 12,09528 + 95,9964 = 180,156 г / моль.
Вызначце элементарную масу, да якой трэба вылічыць працэнт масы. Калі праблема запытвае "працэнт масы", гэта азначае, што вы павінны знайсці масу пэўнага элемента ў злучэнні ў працэнтах ад агульнай масы ўсіх элементаў. Вызначце і запішыце масу элемента. Гэта маса - маса, выражаная ў малярных суадносінах. Гэты лік - лічнік ураўнення працэнтнай масы.
- Прыклад 1: Маса вадароду ў злучэнні складае 201588 г / моль (маса двух моляў атамаў вадароду).
- Прыклад 2: Маса вугляроду ў злучэнні складае 72 062 г / моль (маса шасці моляў атамаў вугляроду).
Заменіце зменныя раўнаннем масавых працэнтаў. Пасля вызначэння значэнняў кожнай зменнай проста заменіце іх раўнаннем, вызначаным на першым этапе: працэнтная маса = (малярная малярная маса / малярная маса злучэння) х 100 .
- Прыклад 1: працэнт масы = (малярная малярная маса / малярная маса злучэння) х 100 = (2,1588 / 18,1528) х 100.
- Прыклад 2: масавы працэнт = (малярная малярная маса / малярная маса злучэння) х 100 = (72 064/180 156) х 100.
Вылічыце працэнт аб'ёму. Цяпер, калі ўраўненне запоўнена, вам трэба толькі вылічыць працэнт масы. Падзяліце масу элемента на агульную масу злучэння, затым памножце на 100. Гэта працэнт масы элемента ў злучэнні.
- Прыклад 1: працэнты масы = (2,01588 / 18,01528) х 100 = 0,111189 х 100 = 11,18%. Такім чынам, масавы працэнт атама вадароду ў малекуле вады складае 11,18%.
- Прыклад 2: масавы працэнт = (малярная малярная маса / малярная маса злучэння) х 100 = (72 064/180 156) х 100 = 0,4000 х 100 = 40,00%. Такім чынам, масавы працэнт атама вугляроду ў малекуле глюкозы складае 40,00%.