Аўтар:
Frank Hunt
Дата Стварэння:
13 Марш 2021
Дата Абнаўлення:
1 Ліпень 2024

Задаволены
- Крок
- Спосаб 1 з 3: Выкарыстанне pH-метра
- Спосаб 2 з 3: з лакмусавай паперай
- Метад 3 з 3: Разуменне рн
Важна вымераць рн - ступень кіслотнасці альбо шчолачнасці - вады. Ваду выкарыстоўваюць расліны і жывёлы, ад якіх мы залежым, і мы п'ем яе кожны дзень. Значэнне pH вады можа сведчыць аб магчымым забруджванні, таму вымярэнне pH вады можа стаць важнай мерай аховы здароўя.
Крок
Спосаб 1 з 3: Выкарыстанне pH-метра
 Калібруйце зонд і глюкометр у адпаведнасці з заводскімі інструкцыямі. Магчыма, вам прыйдзецца адкалібраваць глюкометр, выкарыстоўваючы рэчыва з вядомым значэннем рН. Лічыльнік можна рэгуляваць у адпаведнасці з гэтым рэчывам. Калі вы збіраецеся правяраць ваду за межамі лабараторыі, рэкамендуецца правесці такую каліброўку за некалькі гадзін да палявых выпрабаванняў.
Калібруйце зонд і глюкометр у адпаведнасці з заводскімі інструкцыямі. Магчыма, вам прыйдзецца адкалібраваць глюкометр, выкарыстоўваючы рэчыва з вядомым значэннем рН. Лічыльнік можна рэгуляваць у адпаведнасці з гэтым рэчывам. Калі вы збіраецеся правяраць ваду за межамі лабараторыі, рэкамендуецца правесці такую каліброўку за некалькі гадзін да палявых выпрабаванняў. - Перад выкарыстаннем прамыйце зонд чыстай вадой. Высушыце чыстай тканінай.
 Вазьміце пробу вады і пераліце яе ў чыстую ёмістасць.
Вазьміце пробу вады і пераліце яе ў чыстую ёмістасць.- Вада павінна быць дастаткова глыбокай, каб пагрузіць кончык электрода.
- Пакіньце ўзор на некаторы час, каб тэмпература стабілізавалася.
- Вымяраюць тэмпературу ўзору тэрмометрам.
 Адрэгулюйце глюкометр з улікам тэмпературы ўзору. На адчувальнасць зонда ўплывае тэмпература вады, таму вымярэнне можа быць дакладным толькі пры ўводзе дадзеных аб тэмпературы.
Адрэгулюйце глюкометр з улікам тэмпературы ўзору. На адчувальнасць зонда ўплывае тэмпература вады, таму вымярэнне можа быць дакладным толькі пры ўводзе дадзеных аб тэмпературы.  Змесціце зонд у ўзор. Пачакайце, пакуль метр дасягне раўнавагі. Лічыльнік знаходзіцца ў стабільным стане, калі паказанні стабільныя.
Змесціце зонд у ўзор. Пачакайце, пакуль метр дасягне раўнавагі. Лічыльнік знаходзіцца ў стабільным стане, калі паказанні стабільныя.  Прачытайце вымярэнне рН ўзору. PH-метр дае вынік па шкале 0-14. Калі вада чыстая, значэнне складае каля 7. Запішыце свае вынікі.
Прачытайце вымярэнне рН ўзору. PH-метр дае вынік па шкале 0-14. Калі вада чыстая, значэнне складае каля 7. Запішыце свае вынікі.
Спосаб 2 з 3: з лакмусавай паперай
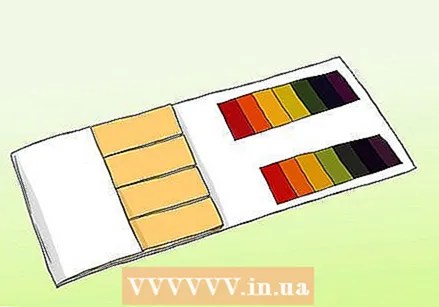 Даведайцеся розніцу паміж pH-паперай і лакмусавай паперай. Вы можаце выкарыстоўваць pH-паперу, каб атрымаць дакладнае адлюстраванне ўзору. Аднак паперу з рн нельга блытаць са звычайнай лакмусавай паперай. І тое, і іншае можна выкарыстоўваць для тэсту на наяўнасць кіслот і асноў, але яны адрозніваюцца па важных параметрах.
Даведайцеся розніцу паміж pH-паперай і лакмусавай паперай. Вы можаце выкарыстоўваць pH-паперу, каб атрымаць дакладнае адлюстраванне ўзору. Аднак паперу з рн нельга блытаць са звычайнай лакмусавай паперай. І тое, і іншае можна выкарыстоўваць для тэсту на наяўнасць кіслот і асноў, але яны адрозніваюцца па важных параметрах. - Паласы рН ўтрымліваюць шэраг індыкатарных палос, якія змяняюць колер пры ўздзеянні раствора. Трываласць кіслот і асноў на кожнай пласціне адрозніваецца. Пасля змены каляровы ўзор можна параўнаць з узорамі, якія ўваходзяць у камплект.
- Лакмусавая папера - гэта папяровая палоска, якая змяшчае кіслату альбо аснову (шчолачную). Самыя распаўсюджаныя паласы - чырвоная (з кіслатой, якая рэагуе з асновамі) і сіняя (з асновай, якая рэагуе з кіслотамі). Чырвоныя палосы становяцца сінімі, калі рэчыва шчолачнае, а сінія палосамі - чырвоным, калі рэчыва кіслае. Лакмусавыя паперы можна выкарыстоўваць у якасці хуткага і простага тэсту, але самыя танныя гатункі не заўсёды даюць дакладную меру трываласці раствора.
 Вазьміце ўзор вады і пераліце ў чыстую ёмістасць. Вада павінна быць дастаткова глыбокай, каб пагрузіць паласу.
Вазьміце ўзор вады і пераліце ў чыстую ёмістасць. Вада павінна быць дастаткова глыбокай, каб пагрузіць паласу.  Апусціце тэст-палоску ў ўзор. Вытрымкі ў некалькі секунд дастаткова. Паласы індыкатара на паперы зменяць колер праз некалькі імгненняў.
Апусціце тэст-палоску ў ўзор. Вытрымкі ў некалькі секунд дастаткова. Паласы індыкатара на паперы зменяць колер праз некалькі імгненняў.  Параўнайце канец тэст-палоскі з каляровай табліцай, якая пастаўляецца з паперай. Колер альбо колеры на картцы павінны адпавядаць колеру альбо колерам тэст-палоскі. Затым каляровая карта суадносіць каляровыя ўзоры з узроўнем pH.
Параўнайце канец тэст-палоскі з каляровай табліцай, якая пастаўляецца з паперай. Колер альбо колеры на картцы павінны адпавядаць колеру альбо колерам тэст-палоскі. Затым каляровая карта суадносіць каляровыя ўзоры з узроўнем pH.
Метад 3 з 3: Разуменне рн
 Даведайцеся, як вызначаюцца кіслоты і асновы. Кіслотнасць і шчолачнасць (тэрмін, які выкарыстоўваецца для апісання падстаў) вызначаюцца іёнамі вадароду, якія яны аддаюць або паглынаюць. Кіслата - гэта рэчыва, якое аддае (альбо "дорыць") іёны вадароду, а аснова - рэчыва, якое паглынае дадатковыя іёны вадароду.
Даведайцеся, як вызначаюцца кіслоты і асновы. Кіслотнасць і шчолачнасць (тэрмін, які выкарыстоўваецца для апісання падстаў) вызначаюцца іёнамі вадароду, якія яны аддаюць або паглынаюць. Кіслата - гэта рэчыва, якое аддае (альбо "дорыць") іёны вадароду, а аснова - рэчыва, якое паглынае дадатковыя іёны вадароду.  Зразумець шкалу рН. Нумар рН выкарыстоўваецца для вымярэння ступені кіслотнасці або шчолачнасці вадараспушчальных рэчываў. У вадзе звычайна аднолькавая колькасць іёнаў гідраксіду (OH−) і іёнаў гідронію (H3O +). Суадносіны гідраксіду і іёнаў гідронію змяняецца пры даданні ў ваду кіслага або шчолачнага рэчыва.
Зразумець шкалу рН. Нумар рН выкарыстоўваецца для вымярэння ступені кіслотнасці або шчолачнасці вадараспушчальных рэчываў. У вадзе звычайна аднолькавая колькасць іёнаў гідраксіду (OH−) і іёнаў гідронію (H3O +). Суадносіны гідраксіду і іёнаў гідронію змяняецца пры даданні ў ваду кіслага або шчолачнага рэчыва. - Звычайна лічыцца шкалой ад 0 да 14 (хоць рэчывы цалкам могуць выходзіць за межы гэтага дыяпазону). Нейтральныя рэчывы налічваюць каля 7, кіслыя - ніжэй за 7, а шчолачныя - вышэй за 7.
- Шкала рН з'яўляецца лагарыфмічнай, што азначае, што цэлалікавыя адрозненні ўяўляюць дзесяціразовую розніцу ў кіслотнасці або шчолачнасці. Напрыклад, рэчыва з рН 2 у дзесяць разоў больш кіслае, чым рэчыва з рН 3, і ў 100 разоў больш кіслае, чым рэчыва з рН 4. Шкала працуе аднолькава з шчолачнымі рэчывамі, з любымі цэлае быццё ўяўляе дзесяціразовую розніцу.
 Даведайцеся, чаму мы правяраем рн вады. Чыстая вада мае pH 7, але галандская вада з-пад крана звычайна мае pH ад 7,5 да 8,3. Вельмі кіслая вада (вада з нізкім значэннем рН) часцей растварае таксічныя хімічныя рэчывы. Яны могуць забруджваць ваду і рабіць яе небяспечнай для ўжывання.
Даведайцеся, чаму мы правяраем рн вады. Чыстая вада мае pH 7, але галандская вада з-пад крана звычайна мае pH ад 7,5 да 8,3. Вельмі кіслая вада (вада з нізкім значэннем рН) часцей растварае таксічныя хімічныя рэчывы. Яны могуць забруджваць ваду і рабіць яе небяспечнай для ўжывання. - Увогуле, рэкамендуецца правяраць pH на месцы. Калі ўзяць пробу вады для лабараторных даследаванняў, вуглякіслы газ (CO2) з паветра можа растварыцца ў вадзе. Раствораны вуглякіслы газ рэагуе з іёнамі ў вадзе і павялічвае кіслотнасць ў асноўных альбо нейтральных растворах. Каб пазбегнуць забруджвання вуглякіслым газам, ваду трэба выпрабаваць на працягу дзвюх гадзін пасля збору.