Аўтар:
Lewis Jackson
Дата Стварэння:
5 Травень 2021
Дата Абнаўлення:
1 Ліпень 2024

Задаволены
Моль - гэта стандартная адзінка вымярэння ў хіміі, якая выкарыстоўваецца для разгляду розных элементаў злучэння. Звычайна маса злучэння вылічаецца ў грамах (г) і павінна быць пераведзена ў малярныя адзінкі. Пераход досыць просты, аднак нам яшчэ трэба зрабіць некалькі важных крокаў. Выкарыстоўваючы прыведзены ніжэй спосаб, вы можаце лёгка пераўтварыць грамы ў молі.
Крокі
Частка 1 з 2: Разлічыце малекулярную масу
Падрыхтуйце неабходныя матэрыялы для вырашэння матэматычнай задачы. Калі ў вас ёсць усе інструменты, лягчэй будзе вырашыць праблему. Вам трэба:
- Аловак і папера. Матэматыка становіцца прасцей, калі вы ўсё запісваеце на паперу. Вам трэба прадставіць усе этапы, каб дасягнуць максімальнага бала.
- Перыядычная сістэма хімічных элементаў: выкарыстоўваецца для вызначэння масы атамаў элементаў.
- Кішэнны калькулятар: выкарыстоўваецца для вылічэння складаных лікаў.

Вызначце, якія элементы ў злучэнні трэба пераўтварыць у малярныя адзінкі. Першым этапам разліку малекулярнай масы з'яўляецца вызначэнне элементаў, якія складаюць злучэнне. Гэта лёгка, таму што абрэвіятура элементаў складае ўсяго адзін-два сімвалы.- Калі рэчыва скарочана двума літарамі, першая літара будзе напісана з вялікай літары, а другая - з малой. Прыклад: Mg - абрэвіятура элемента магній.
- Злучэнні NaHCO3 складаецца з чатырох элементаў: натрыю (Na), вадароду (H), вугляроду (C) і кіслароду (O).
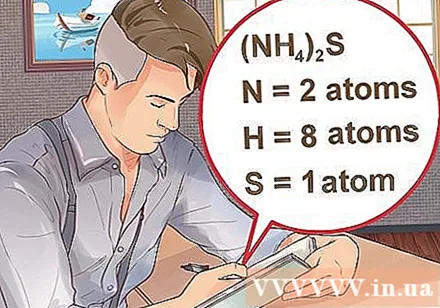
Вызначце колькасць атамаў для кожнага элемента ў злучэнні. Вам трэба ведаць атамны нумар кожнага рэчыва ў злучэнні, каб вылічыць малекулу масы гэтага злучэння. Невялікая лічба побач з абрэвіятурай элемента ўяўляе атамны нумар элемента.- Прыклад: злучэнне Н2O мае два атамы вадароду і адзін атам кіслароду.
- Калі ў дужках злучэнне напісана, за якім ідзе невялікі індэкс, кожны інгрэдыент у дужках памнажае індэкс. Прыклад: злучэнне (NH4)2S складаецца з двух атамаў N, васьмі атамаў Н і аднаго атама S.

Запішыце кубічную атамную паперу для кожнага элемента. Выкарыстанне перыядычнай табліцы - гэта самы просты спосаб знайсці кубічны атам элемента. Пасля знаходжання элемента ў перыядычнай табліцы вы ўбачыце атамную масу адразу пад значком элемента.- Напрыклад, кубічны атам кіслароду складае 15,99.
Разлічыце малекулярную масу. Масавая малекула рэчыва роўная колькасці атамаў кожнага элемента, памножанага на масавы атам гэтага элемента. Гэта колькасць неабходна для пераўтварэння ў грам у малярны.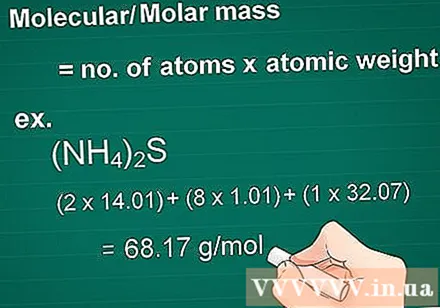
- Спачатку памножце атамны нумар кожнага элемента ў злучэнні на яго масавы атам.
- Затым складзіце масу элементаў у злучэнні.
- Прыклад: Малекулярная маса злучэння (NH4)2S = (2 х 14,01) + (8 х 1,01) + (1 х 32,07) = 68,17 г / моль.
- Малекулярная маса таксама вядомая як малярная маса.
Частка 2 з 2: Пераўтварэнне грамаў у моль
Наладзьце формулу пераўтварэння. Каб знайсці колькасць молей злучэння, падзяліце колькасць грамаў злучэння на малярную масу гэтага злучэння.
- Формула: колькасць радзімак = маса (грам) / малярная маса злучэння (грам / моль)
Падстаўце лічбы ў формулу. Пасля наладжвання правільнай формулы наступным крокам з'яўляецца замена вылічаных лікаў формулай. Калі вы хочаце пераканацца, што дадзеныя знаходзяцца ў правільным становішчы, вы можаце праверыць гэта, падаўшы блок. Калі пасля прастаты астатнім блокам з'яўляюцца радзімкі, значыць, вы правільна настроены.
Рашы ўраўненне. З дапамогай калькулятара падзяліце масу на кубічную малекулу рэчыва ці злучэння. Каэфіцыентам будзе колькасць молей шуканага рэчыва альбо злучэння.
- Напрыклад, вы павінны ўзяць 2 г вады (H2O) і папрасіць перавесці яго ў малярныя адзінкі. У нас малярная маса H2Аб складае 18 г / моль. Падзяліце 2 на 18, у вас атрымаецца 0,1111 моль H2O.
Парада
- Не забудзьцеся далучыць да адказаў імя элемента або злучэння.
- Калі вам будзе прапанавана прадставіць практыкаванне або віктарыну, пераканайцеся, што вы дакладна паказваеце свае адказы, кружачы альбо малюючы поле вакол адказаў.
Што вам трэба
- Хімічная табліца Мендзялеева
- Аловак
- Папера
- Кампутар
- Праблемы хіміі